烷烴的通式:
烷烴的通式為CnH2n+2
相關高中化學知識點:環(huán)烷烴(環(huán)己烷、環(huán)丙烷等)
環(huán)烷烴:
(1)通式:CnH2n
(2)性質:隨碳原子數的增加,熔沸點升高
①催化加氫

②加鹵素、鹵化氫

③取代反應

④氧化反應

相關高中化學知識點:甲烷
甲烷:
(1)結構式:
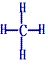 、球棍模型:
、球棍模型: 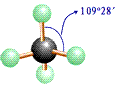 、比例模型:
、比例模型: 
空間構型為正四面體。
(2)物理性質:無色無味的氣體,密度0.717g/L,記憶溶于水。
(3)化學性質:通常情況下甲烷比較穩(wěn)定,與高錳酸鉀等強氧化劑不反應,與強酸強堿不反應,可發(fā)生氧化反應、取代反應
①氧化反應:CH4+O2
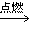 CO2+2H2O
CO2+2H2O ②取代反應:CH4+Cl2
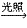 CH3Cl+HCl,甲烷在光照條件下反應,現象:試管內氣體顏色逐漸變淺,試管壁上有油狀液滴,試管中有少量白霧。甲烷中四個氫原子都可以與氯氣發(fā)生取代,甲烷的4中氯代產物都不溶于水,常溫下,一氯甲烷是氣體,其他都為液體,三氯甲烷俗稱氯仿。
CH3Cl+HCl,甲烷在光照條件下反應,現象:試管內氣體顏色逐漸變淺,試管壁上有油狀液滴,試管中有少量白霧。甲烷中四個氫原子都可以與氯氣發(fā)生取代,甲烷的4中氯代產物都不溶于水,常溫下,一氯甲烷是氣體,其他都為液體,三氯甲烷俗稱氯仿。 甲烷與氯氣等鹵素單質反應的注意事項:
1.反應條件為光照,在室溫或暗處不發(fā)生反應,但不能用強光直接照射,以免引起爆炸。
2.甲烷與溴蒸氣、碘蒸氣等純鹵素也能發(fā)生類似反應,但不能與溴水、碘水發(fā)生反應。
3.甲烷與氯氣的反應是一種連鎖反應,不會停留在某一步,因此產物一般是五種物質的混合物。
4.CH4與Cl2在光照條件反應,生成物中HCl的物質的量最多。
5.1mol有機物CxHy與Cl2發(fā)生完全取代反應時,消耗Cl2的物質的量為ymol。
原子共面的判斷方法:
判斷有機物分子中的原子是否共面,首先要熟悉常見的分子構型。如甲烷分子(CH4)為正四面體結構,其分子中最多有三個原子共面;乙烯分子 (CH2=CH2)中的所有原子共面;苯分子(C6H6)中的所有原子共面。在判斷有機物分子中原子共面情況時,把要分析的分子看做是簡單的常見分子的衍生物,即復雜問題簡單處理
(1)在甲烷分子中,一個碳原子和任意兩個氫原子可確定一個平面,即甲烷分子中有且只有三個原子共面。當甲烷分子中的某個氫原子被其他原子或原子團取代時,則代替該氫原子的原子一定在原來的平面上。
(2)乙烯分子中所有原子在同一平面內,鍵角為 120。。當乙烯分子中的某個氫原子被其他原子或原子團取代時,則代替該氫原子的原子一定在乙烯分子所在的平面內。
(3)苯分子中所有原子在同一個平面內,鍵角為 120。。當苯分子中的某個氫原子被其他原子或原子團取代時,則代替該氫原子的原子一定在苯分子所在的平面內。說明有機化合物分子中的單鍵(包括碳碳單鍵、碳氫單鍵、碳氧單鍵等)可以旋轉;而雙鍵、三鍵不能旋轉
相關高中化學知識點:烷烴的通性
烷烴的通性:
(1)物理性質:隨著分子中碳原子數的遞增,熔沸點逐漸升高,相對密度逐漸增大,常溫下存在狀態(tài),由氣態(tài)逐漸過渡到液態(tài)、固態(tài)。
(2)烷烴的化學性質:可發(fā)生氧化、取代、分解等反應。
烷烴的氧化反應:烷烴燃燒生成二氧化碳和水。CxHy+(x+0.25y)O2
 xCO2+0.5yH2O
xCO2+0.5yH2O烷烴的取代反應:烷烴在光照下可發(fā)生取代反應。CnH2n+2+Cl2
 CnH2n+1Cl+HCl
CnH2n+1Cl+HCl 烷烴的分解反應:烷烴在高溫條件下能夠裂解。如:C4H10
 CH2=CH2+CH3CH3
CH2=CH2+CH3CH3 本文來自:逍遙右腦記憶 http://m.bjhkkj.cn/gaozhong/683458.html
相關閱讀:如何正確看待一模、二模考試